En el presente artículo analizamos de forma detallada el uso de SARMs.
El uso de sustancias para mejorar el rendimiento y/o composición corporal en deportistas se ha extendido durante los últimos años, entre las sustancias más utilizadas se encuentran los esteroides anabólicos androgénicos (EAA).
Diversas investigaciones han reportado gran variedad de efectos secundarios debido al uso de estos fármacos; como alternativa a los EAA, surgen los moduladores selectivos de los receptores androgénicos, mejor conocidos por sus siglas en ingles como SARMs.
Aunque estas sustancias todavía se encuentran en investigación, se pueden encontrar en diversas tiendas de suplementos y en internet, donde se afirma que pueden tener efectos como el aumento de masa muscular y pérdida de grasa, sin los efectos secundarios de los EEA.
¿Qué son los SARMs?
Los SARMs son sustancias que poseen una alta especificidad en los receptores androgénicos, destacando su efecto sobre el músculo esquelético y los huesos, son débiles agonistas o antagonistas de la respuesta andrógena en tejidos como las glándulas sebáceas y la próstata y se encuentran disponibles para administrarse de forma oral.
Ya que el requisito más importante para un SARM es la selectividad del tejido, cualquier ligando que cumpla el criterio, sea Uso de anabolizantes esteroideos o no esteroide agonista o antagonista, se considera SARM (1).
Los SARM no son esteroides anabólicos ; más bien, son ligandos sintéticos que se unen a los receptores de andrógenos (AR). Dependiendo de su estructura química, funcionan como agonistas completos, agonistas parciales o antagonistas.
Origen de los SARMs
Los SARMs esteroideos se empezaron a desarrollar en la década de 1940, mediante la modificación de la molécula de testosterona (2).
La suplementación con testosterona aumenta la masa muscular esquelética y la fuerza en hombres sanos con déficit de andrógenos (3,4), eugonadicos jóvenes (5,6), personas mayores (7) y personas con otros trastornos crónicos (8,9).
Los efectos anabólicos de la testosterona sobre la masa muscular y la fuerza se relacionan directamente con la dosis de testosterona (6,9-11).
Por tanto, los efectos de ganancia muscular y fuerza son sustanciales a la dosis; se ha observado que la administración de dosis suprafisiológicas de testosterona está asociada a varios efectos adversos como eritrocitosis, edema de piernas y problemas de la próstata (12).
A pesar de los inconvenientes por la suplementación de testosterona, también se han descubierto potenciales beneficios en enfermedades crónicas asociadas con la edad y en la osteoporosis, impulsando a las compañías farmacéuticas el desarrollo de SARMs.
Estructuralmente los SARMs se pueden clasificar en esteroideos o no esteroideos, los primeros se forman mediante la modificación de la estructura química de la testosterona (13).
Incrementa tu rendimiento y consigue tu mejor nivel cuidando tu alimentación y ayudándote de suplementación. Te mostramos todas las claves para mejorar tu alimentación de deportista
Todas las claves para mejorar tu alimentación de deportista. Mejora tus conocimientos de forma práctica y descubre las nuevas tendencias en nutrición deportiva.
¿Son seguros los SARMs?
No existe suficiente evidencia científica que confirme que los SARMs son efectivos y seguros, puesto la gran parte se encuentra en fases de investigación, y aunque existen en el mercado de suplementos e internet, es posible que puedan poner en riesgo la salud.
A continuación analizamos las investigaciones recientes sobre los SARMs:
Evidencias científicas en relación al consumo de SARMs
Se han sometido diversos SARMs a investigaciones, convirtiéndose en ensayos clínicos de fase 1, 2 y 3, y aunque se han encontrado resultados prometedores con respecto a la selectividad del tejido.
La mayor parte de estos datos han permanecido inéditos por parte de las compañías farmacéuticas, dificultando la comparación entre la potencia y selectividad de los diferentes SARMs (14,15).
Varios de los SARMs de primera generación se encuentran en la fase 1 de ensayos clínicos. Estos compuestos se están destinando al tratamiento de osteoporosis temprana, caquexia por cáncer y limitaciones funcionales asociadas al envejecimiento.
En las dosis administradas los SARMs de primera generación han producido ganancias moderadas (1 a 1.5 kg) en la masa muscular de sujetos voluntarios sanos.
Sin embargo estas ganancias no se acercan a las obtenidas con dosis suprafisiológicas de enantato de testosterona (5-7 kg con dosis de 300 y 600 mg) en un tiempo promedio de 4-6 semanas (13).
Actualmente se encuentran disponibles en el mercado una serie de SARMs como la flutamida, nilutamida y bicalutamida y una nueva serie se encuentra en vías de desarrollo para el tratamiento de cáncer o caquexia asociada a enfermedades crónicas, sarcopenia y osteoporosis.
El GTx-024 (ostarine, enobosarm) es un nuevo SARM que ha sido sometido a ensayos clínicos de fase 3 para la prevención de la atrofia muscular asociada al cáncer de pulmón (14).
En la misma línea, con resultados prometedores, se encuentra el VK-5211 (antes conocido como LGD-4033), este compuesto fue sometido a ensayos clínicos de fase 1 en 2009 y los resultados se publicaron en 2013 (15).
El VK-5211 será sometido a estudios clínicos de fase 2 para conocer los efectos sobre el desgaste muscular por cáncer, enfermedades agudas o fractura de cadera (1).
En un estudio de fase 1 con una duración de 12 semanas, el MK-0773 ha demostrado incrementar la masa libre de grasa (MLG) sin androgenización de la piel (16).
En otro estudio de fase 2a con una duración de 6 meses, se encontró un aumento de la MLG con un incremento estadísticamente significativo de la fuerza y del rendimiento, aunque la diferencia media entre los grupos placebo y MK-0773 no fue significativa (17).EL DT ( antes GLPG0492), ha mostrado buena tolerabilidad oral en ensayos clínicos de fase 1 y en un estudio de fase 2a para distrofia muscular (1).
El GTx-024 reportó resultados positivos aumentando la MLG y la funcionalidad en pacientes con cáncer de pulmón en ensayos de fase 3 (18, 19).
Se realizó un estudio de fase 2, doble ciego, controlado con placebo durante 12 semanas, donde el GTx-024 fue administrado a 120 personas sanas de edad avanzada ( hombres y mujeres), en 5 grupos aleatorizados: placebo, 01 mg, 0.3 mg 1 mg y 3 mg.
Los parámetros monitoreados en la investigación fueron: crecimiento del vello en mujeres (hirsutismo),la producción de sebo, los niveles hormonales séricos, los parámetros lipídicos en suero y la función hepática.
Las alteraciones más notables se observaron en los niveles séricos de lípidos y en las hormonas sexuales. Se reportaron descensos del HDL del 17 y 27% para las dosis de 1 y 3 mg respectivamente.
De igual forma se observó una disminución significativa, pero no dosis-dependiente del colesterol total.
Las dosis superiores a 1 mg disminuyeron los niveles de triglicéridos en mas del 10% de los niveles basales, sin embargo no se consideró una disminución estadísticamente significativa.
En los hombres los niveles de testosterona disminuyeron significativamente, aunque los niveles de testosterona libre, dihidrotestosterona (DHT), estradiol, hormona folículo estimulante (FSH) y luteinizante (LH), no mostraron diferencias entre los grupos.
En las mujeres se redujeron la LH y la FSH con las dosis de 3 mg .En esta investigación el 8.3% (8/96) de los participantes mostraron un aumento transitorio de los niveles de alanina transaminasa (ALT), al suspender el fármaco se recuperaron los niveles basales de la enzima a excepción de un participante (20).
Se realizó otra investigación similar con el mismo SARMs, en donde no se reportaron efectos adversos graves o potencialmente mortales, aunque se encontraron aumentos transitorios del ALT en un 15% (3/20) de los sujetos que utilizaron 3 mg del fármaco (21).
Se realizó con el MK0773, un ensayo clínico aleatorizado de fase 2a, doble ciego, controlado con placebo con una duración de 6 meses, en mujeres mayores de 65 años con sarcopenia.
Aunque el fármaco fue bien tolerado de manera general, se encontraron varios efectos adversos como aumento en los niveles de ALT y aspartato aminotransferasa(AST), del hematocrito y de la presión arterial, no se encontraron incrementos de los indicadores de puntuación de acné o hirsutismo comparado con el grupo placebo (17).
En el 2012 se publicaron los resultados de un estudio de fase 1 que evaluó la seguridad y tolerabilidad del LGD-4033, fue un estudio clínico, aleatorizado, doble ciego, controlado con placebo, en donde se administró el fármaco a hombres sanos de forma oral durante 21 días en dosis de 0.1, 0.3 y 1 mg.
Se midieron niveles hormonales en sangre de forma constante hasta 35 días después de la administración de la sustancia, se midió LH, FSH, hormona adrenocorticotrópica, cortisol, testosterona libre, testosterona total y los niveles de lípidos sanguíneos: Colesterol, HDL, LDL y triglicéridos.
Los resultados indicaron que la incidencia de efectos adversos fue similar en los sujetos que utilizaron LGD-4033 y los que consumieron placebo, concluyendo que el fármaco no produce efectos adversos graves en la función hepática, parámetros hematológicos, antígeno prostático específico (PSA) o en el electrocardiograma (22).
¿Qué diferencias hay entre los esteroides anabólicos y los SARMs?
Los SARM son similares a los esteroides , pero no son lo mismo. Ambos funcionan al unirse a sus receptores de andrógenos, lo que desencadena cambios en su ADN que aumentan la capacidad de crecimiento de sus músculos.
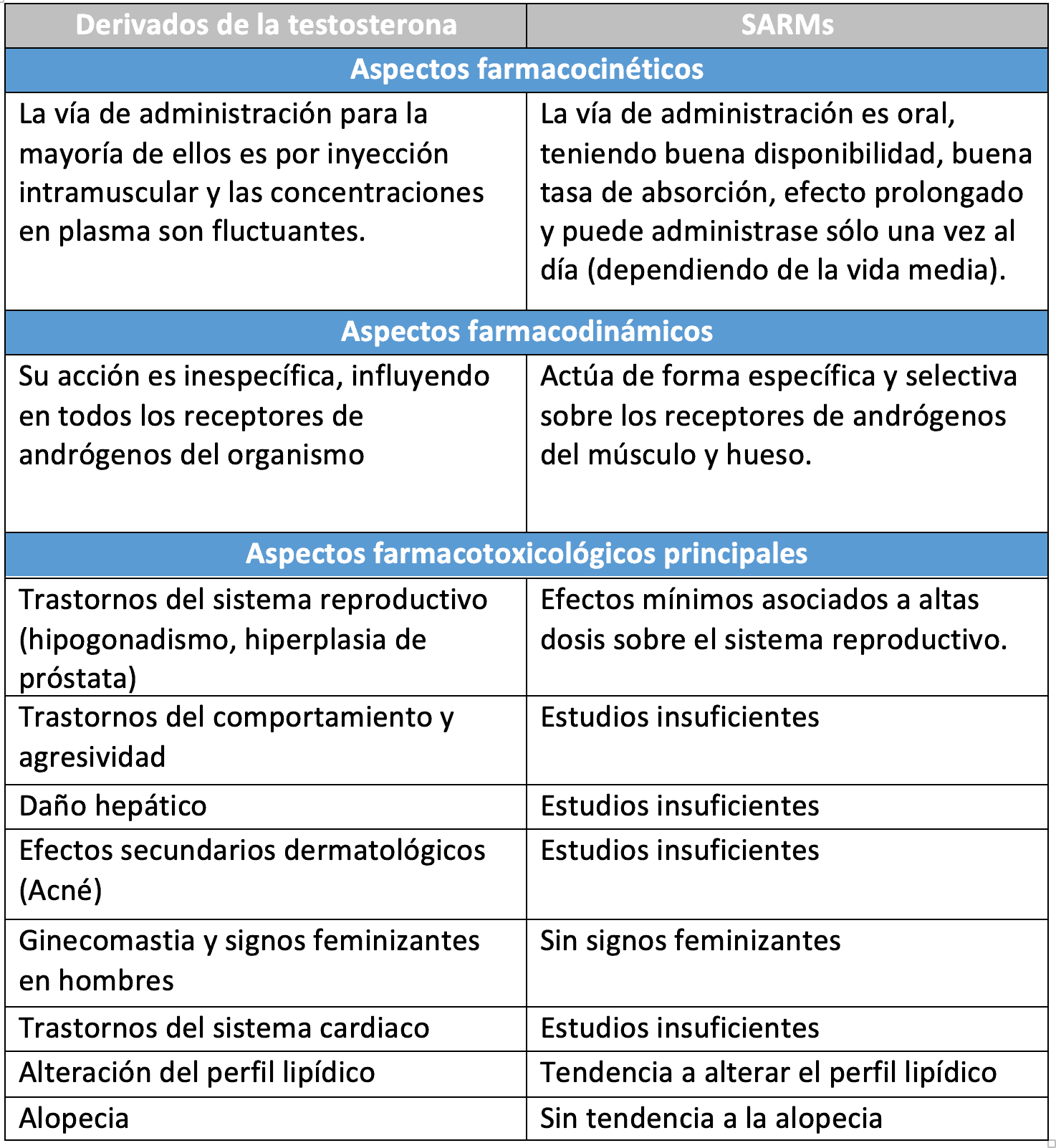
Respecto al perfil farmacológico, como vemos en la tabla 1, se puede concluir que estas sustancias no disponen de un perfil farmacotoxicológico definido de forma clara.
La ventaja más potencial de los SARMs radica en que no tienen estructura esteroidea como los anabolizantes, evitando efectos secundarios a nivel de tejidos u órganos como la próstata.
Además, actúan como agonistas de los receptores de andrógenos como antes hemos comentado.
¿Cuáles son los efectos secundarios de los SARMs?
El consumo de SARMs puede producir efectos secundarios potencialmente mortales, debido a toxicidad hepática. Según apuntan algunos estudios, pueden incrementar el riesgo de ataque cardiaco y accidente cerebrovascular.
Un estudio reciente en la Revista de la Asociación Médica Estadounidense evaluó la composición química de los productos que se comercializan como SARM.
Descubrieron que solo la mitad de ellos contenían SARM. Alrededor del 60 por ciento contenía ingredientes diferentes de los que aparecían en la etiqueta.
Casi el 10 por ciento de los productos probados no contenían ningún ingrediente activo.
¿Puedo consumir SARMs para incrementar músculo?
Los consumidores deberían de evitar consumir SARMs, actualmente no existe evidencia científica suficiente que respalde su consumo de forma segura.
Antes de iniciarse en el consumo de estas sustancias deberían consultar a un profesional de la salud, aunque la evidencia parece respaldar que son sustancias tóxicas que debemos evitar.
Si buscas un suplemento saludable que incremente tu testosterona y tu masa muscular de forma natural te recomendamos el tribulus terrestris.
👌 EXCELENTE FÓRMULA a base de extracto natural de los frutos del Tribulus Terrestris con 90% de Saponinas. | Ayuda a aumentar la testosterona, incrementar la masa muscular, la fuerza, la resistencia y el rendimiento físico. | GRAN CANTIDAD DE PRODUCTO AL MEJOR PRECIO: Ofrecemos 180 cápsulas veganas por bote, suministro para 2 meses.
Conclusiones sobre los SARMs en el culturismo
Los SARMs actúan únicamente como agonistas de los receptores de andrógenos ubicados en huesos y músculos, lo que permite disociar la acción anabólica de la acción androgénica.
Aunque los resultados obtenidos con los SARMs son prometedores, es necesario realizar más estudios para evaluar la eficacia y seguridad de estos fármacos.
Es de gran importancia recordar que tanto los EAA como los SARMs fueron desarrollados para el tratamiento de diversas enfermedades en donde existe un problema hormonal o una gran pérdida de masa muscular.
Por lo tanto hasta el momento no existen investigaciones experimentales que usen SARMs o EAA como ayudas ergogénicas o como productos para mejorar la composición corporal.
No existe suficiente evidencia científica que confirme que los SARMs son efectivos y seguros, puesto la gran parte se encuentra en fases de investigación, y aunque existen en el mercado de suplementos e internet, es posible que sean falsos o que puedan poner en riesgo la salud.
Los SARMs son medicamentos en investigación que se han estudiado durante muchos años, pero ninguno ha recibido la aprobación de las administraciones competentes, incluso para condiciones en las que los beneficios podrían superar cualquier riesgo significativo.
Gran parte de la evidencia con respecto a los beneficios de mejora del rendimiento y la seguridad general de los SARMs es anecdótica y no se basa en una investigación científica consolidada.
Los SARMs más populares actualmente en el mercado incluyen Ostarine (MK-2866), Ligandrol (LGD-4033), Testolone (RAD-140) y Andarine (GTx-007, S4).
Bibliografía
- Choi, S. M., & Lee, B. M. (2015). Comparative safety evaluation of selective androgen receptor modulators and anabolic androgenic steroids. Expert Opinion on Drug Safety, 14(11), 1773-1785.
- George, S., Petit, G. H., Gouras, G. K., Brundin, P., & Olsson, R. (2013). Nonsteroidal selective androgen receptor modulators and selective estrogen receptor β agonists moderate cognitive deficits and amyloid-β levels in a mouse model of Alzheimer’s disease. ACS chemical neuroscience, 4(12), 1537-1548.
- Ramaraj, P., Artaza, J. N., Sinha-Hikim, I., & Taylor, W. E. (2015). Effect of Androstenedione on Adipogenesis in Murine C3H10T1/2 Mesenchymal Cells. Open Journal of Endocrine and Metabolic Diseases, 5(02), 9.
- Wang, X., Smith, G. I., Patterson, B. W., Reeds, D. N., Kampelman, J., Magkos, F., & Mittendorfer, B. (2012). Testosterone increases the muscle protein synthesis rate but does not affect very-low-density lipoprotein metabolism in obese premenopausal women. American Journal of Physiology-Endocrinology and Metabolism, 302(6), E740-E746.
- Bhasin, S., Storer, T. W., Berman, N., Callegari, C., Clevenger, B., Phillips, J. & Casaburi, R. (1996). The effects of supraphysiologic doses of testosterone on muscle size and strength in normal men. New England Journal of Medicine, 335(1), 1-7.
- Bhasin, S., Woodhouse, L., Casaburi, R., Singh, A. B., Bhasin, D., Berman, N. & Dzekov, J. (2001). Testosterone dose-response relationships in healthy young men. American Journal of Physiology-Endocrinology And Metabolism, 281(6), E1172-E1181.
- Casaburi, R., Bhasin, S., Cosentino, L., Porszasz, J., Somfay, A., Lewis, M. I. & Storer, T. W. (2004). Effects of testosterone and resistance training in men with chronic obstructive pulmonary disease. American journal of respiratory and critical care medicine, 170(8), 870-878.
- Johansen, K. L., Mulligan, K., & Schambelan, M. (1999). Anabolic effects of nandrolone decanoate in patients receiving dialysis: a randomized controlled trial. Jama, 281(14), 1275-1281.
- Bhasin, S., Woodhouse, L., Casaburi, R., Singh, A. B., Mac, R. P., Lee, M. & Magliano, L. (2005). Older men are as responsive as young men to the anabolic effects of graded doses of testosterone on the skeletal muscle. The Journal of Clinical Endocrinology & Metabolism, 90(2), 678-688.
- Woodhouse, L. J., Reisz-Porszasz, S., Javanbakht, M., Storer, T. W., Lee, M., Zerounian, H., & Bhasin, S. (2003). Development of models to predict anabolic response to testosterone administration in healthy young men. American Journal of Physiology-Endocrinology and Metabolism, 284(5), E1009-E1017..
- Storer, T. W., Magliano, L., Woodhouse, L., Lee, M. L., Dzekov, C., Dzekov, J. & Bhasin, S. (2003). Testosterone dose-dependently increases maximal voluntary strength and leg power, but does not affect fatigability or specific tension. The Journal of Clinical Endocrinology & Metabolism, 88(4), 1478-1485.
- Calof, O. M., Singh, A. B., Lee, M. L., Kenny, A. M., Urban, R. J., Tenover, J. L., & Bhasin, S. (2005). Adverse events associated with testosterone replacement in middle-aged and older men: a meta-analysis of randomized, placebo-controlled trials. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences, 60(11), 1451-1457.
- Bhasin, S., & Jasuja, R. (2009). Selective androgen receptor modulators (SARMs) as function promoting therapies. Current opinion in clinical nutrition and metabolic care, 12(3), 232.
- Srinath, R., & Dobs, A. (2014). Enobosarm (GTx-024, S-22): a potential treatment for cachexia. Future Oncology, 10(2), 187-194.
- Basaria, S., Collins, L., Dillon, E. L., Orwoll, K., Storer, T. W., Miciek, R., … & Gordon, G. (2013). The safety, pharmacokinetics, and effects of LGD-4033, a novel nonsteroidal oral, selective androgen receptor modulator, in healthy young men. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences, 68(1), 87-95.
- Marcantonio, E. E., Witter, R. E., Ding, Y., Xu, Y., Klappenbach, J., Wang, Y., & Stoch, S. A. (2010). A 12-Week Pharmacokinetic and Pharmacodynamic Study of Two Selective Androgen Receptor Modulators (SARMs) in Postmenopausal Subjects. Endocrine Reviews Supplement, 31 (1), 872.
- Papanicolaou, D. A., Ather, S. N., Zhu, H., Zhou, Y., Lutkiewicz, J., Scott, B. B., & Chandler, J. (2013). A phase IIA randomized, placebo-controlled clinical trial to study the efficacy and safety of the selective androgen receptor modulator (SARM), MK-0773 in female participants with sarcopenia. The journal of nutrition, health & aging, 17(6), 533-543.
- Srinath, R., & Dobs, A. (2014). Enobosarm (GTx-024, S-22): a potential treatment for cachexia. Future Oncology, 10(2), 187-194.
- Dalton, J. T., Taylor, R. P., Mohler, M. L., & Steiner, M. S. (2013). Selective androgen receptor modulators for the prevention and treatment of muscle wasting associated with cancer. Current opinion in supportive and palliative care, 7(4), 345-351.
- Dalton, J. T., Barnette, K. G., Bohl, C. E., Hancock, M. L., Rodriguez, D., Dodson, S. T., & Steiner, M. S. (2011). The selective androgen receptor modulator GTx‐024 (enobosarm) improves lean body mass and physical function in healthy elderly men and postmenopausal women: results of a double‐blind, placebo‐controlled phase II trial. Journal of cachexia, sarcopenia and muscle, 2(3), 153-161.
- Dobs, A. S., Boccia, R. V., Croot, C. C., Gabrail, N. Y., Dalton, J. T., Hancock, M. L., & Steiner, M. S. (2013). Effects of enobosarm on muscle wasting and physical function in patients with cancer: a double-blind, randomised controlled phase 2 trial. The lancet oncology, 14(4), 335-345.
- Basaria, S., Collins, L., Dillon, E. L., Orwoll, K., Storer, T. W., Miciek, R., . & Gordon, G. (2013). The safety, pharmacokinetics, and effects of LGD-4033, a novel nonsteroidal oral, selective androgen receptor modulator, in healthy young men. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences, 68(1), 87-95.






Hola mi experiencia es Ni se les ocurra usar Sarms, consumí 15 mg de rad140 x 1 mes, y luego combine 10 mg ligandrol y 10 rad 140 x otro mes, total 2 meses y me cree una hepatoxicidad terrible, ictericia color amarillento en la piel y ojos, prurito intenso, insomnio, mi colesterol ldl aumento a la locura, mi triglicéridos, tenía riesgo coronario de 7% , mis traferasa, fosfata alcalina elevadisimas, y lo q causa la ictericia es la hiberbilirrubina total la cual paso de 3 MG/dl a 7 mg/do y luego a 10mg/dl y ahora está en 23mg/dl mi orina super amarilla y heces totalmente claras, es terrible ni se les ocurra, x el otro lado los efectos de fuerza y musculatura si son inmediatos pase se levanta 120lbs en banca plana a 220 lbs, pero ahora pa que si perdí todo lo que gane, me ha afectado psicológicamente xq andar amarillo en la calle da pena y pues he gastado más de $1500 dólares en exámenes, colangio resonancia, medicinas q por cierto tome Meneparol y Sylimarina 70 mg, y colestiramina 4mg para el prurito, aunque a veces no funciona y tengo que usar algún otro antihistamínico cómo difenidramina y lorazepam para poder dormir, sin mencionar lo horrible que se pone tu piel de tanto rascarte, No chicos no lo hagan se los digo yo que he sufrido x esto, supuestamente 3 a 4 meses pa regresar a la normalidad apenas voy x el primer mes
Gracias por el artículo, la verdad es que estaría bien tener un poco más información al respecto. Yo por mi parte he empezado a probar con este producto andarine (https://www.bestsarms.net/es/producto/andarine-s-4/) y por ahora todo bien, muy contento con los resultados.
Hola buenas, un placer saludarte, la verdad es que tengo curiosidad por saber como te fue con el tema del SARMs porque estoy pensando en probarlo pero no tengo ninguna referencia, gracias por tu atención!
hola buenas me gustaria saber con que edad podría usar sarms… sirve tanto para hombre para mujer ?