El estrés regula la liberación del cortisol en el torrente sanguíneo. Su hipersolicitación o excesiva liberación puede desarrollar determinados trastornos a largo plazo, como por ejemplo, cambios en la conducta alimentaria, atracones o desorden en la alimentación.
En el siguiente artículo, abordaremos en detalle como el exceso de cortisol puede afectar directamente al producir hambre emocional, factor que suele predominar en mujeres y se traduce en un mayor consumo de alimentos de alta densidad energética con los consecuentes cambios fisiológicos y en la composición corporal.
¿Qué es el cortisol? y ¿Cuál es su influencia en el metabolismo?
El cortisol es una hormona esteroidea producida por el eje y centro hipotálamopituitario-adrenal una parte fundamental en la conexión del sistema neuro- endócrino (1).
La activación de este centro se realiza por la hormona adrenocorticotrofina secretada en la hipófisis con la finalidad de estimular la hormona corticotrofina y la arginina vasopresina, esto con el objetivo de producir y liberar cortisol en la glándula suprarrenal.
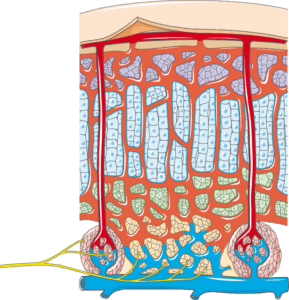
La producción de cortisol se lleva a cabo mediante la retroalimentación y secreción de adrenocorticotrofina, por tanto, ésta hormona trabaja de forma directa sobre la hipófisis, así como también lo hace sobre el hipotálamo, conformando en definitiva, lo que seria el eje hipotálamo-hipófisis-adrenal (2).
El aumento excesivo del estrés a nivel fisiológico y psicológico, va a desencadenar una cascada o serie de alteraciones fisiológicas que van a producir un descenso de glucocorticoides en sangre, activa el eje hipotálamo-hipófisis-adrenal, resultando esto en la liberación de cortisol plasmático.
Por otro lado, hay que remarcar que la secreción de cortisol también se relaciona con el ritmo circadiano, presentando una mayor secreción por la mañana y el nivel más bajo por la noche.
Además, dicha liberación de cortisol va a estar ligada fuertemente por los horarios de mayor actividad, ejercicio y los horarios de las comidas, así como también por la iluminación ambiental o la luz artificial (3).
Estrés y su relación con la elevación de cortisol
El estrés crónico, principalmente a través de la desregulación del eje hipotalámico-hipofisario-adrenal, promueve a la acumulación de grasa visceral.
A su vez, el sobrepeso graso promueve un estado sistémico de inflamación de bajo grado, el cual es mediado por una mayor secreción de adipocinas (hormonas liberadas por adipocitos blancos), que pueden estimular y alterar crónicamente la liberación de cortisol y aumento del estrés.
Este círculo vicioso, probablemente iniciado por la disfunción del tejido adiposo visceral, es uno de los principales desencadenantes del síndrome metabólico y el sobrepeso graso. Ya que, la liberación excesiva de glucocorticoides se asocia fuertemente con un aumento del hambre emocional (4).
El estrés entonces, es capaz de promover variaciones o desajustes en la manera en que se percibe o interactúa con el ambiente, produciendo serios cambios en la conducta alimentaria y en la función orgánica.
Es decir, la conducta alimentaria es consecuencia de un mecanismo fisiológico que busca la homeostasis con la finalidad de cubrir las necesidades energéticas a través de la ingesta de alimentos, pero esta a su vez, puede ser vulnerada por factores neurohumorales involucrados por la acción fisiológica del estrés o por el tipo de alimento ingerido.
Factores y consecuencias fisiológicas que en combinación pueden ocasionar un desbalance en la composición corporal, perdida del tejido muscular, un aumento en el almacenamiento de tejido adiposo, inflexibilidad metabólica y un acceso crónico a multiplicidad de patologías metabólicas (5, 6, 7).
Efectos negativos del cortisol excesivo sobre la alimentación
Los cambios negativos en el estado de animo producidos por el estrés crónico determinan en gran medida el aumento en el consumo de alimentos, en su mayoría multiprocesados o alimentos de mayor palatabildad, lo cual en definitiva, produce una grave alteración en el aporte energético (8).
.
Pese a esto, otros estudios observaron por mecanismos similares una ingesta menor ante un aumento excesivo del cortisol en el torrente sanguíneo, lo que demuestra en definitiva, que cada organismo responde diferente, pero produciendo de todas formas un desequilibrio metabólico (9).
Por otro lado, parece ser que los glucocorticoides hiperactivan la señalización de vías relacionadas con el placer, esto produciría un cambio preferencial hacia los alimentos altamente palatables siendo ricos en grasas saturadas, carbohidratos refinados y de una alta densidad energética, lo que en definitiva produce un balance calórico positivo (10).
Este hambre emocional se debería, entonces, a que la activación de los mecanismos de recompensa hacia los alimentos es menor cuando el cortisol está elevado, produciendo una mayor sensibilidad de los circuitos centrales y aumentando los antojos de aquellos alimentos de fácil alcance y de características poco nutricionales, propios de un ambiente obesogenico (11).
Ver esta publicación en Instagram
Hambre y emociones negativas
El hambre emocional se puede definir como un estado en donde el sujeto desea comer un alimento en respuesta a una serie de emociones negativas y que no necesariamente responden a una necesidad fisiológica.
Estos mecanismos son alterados principalmente por ansiedad, depresión o la soledad. Pese a esto, algunos estudios muestran que emociones positivas también podrían ocasionar un aumento en la ingesta de alimentos o en los mecanismos de recompensa, pero esto sucede en menor medida aunque también a largo plazo puede ocasionar efectos adversos de carácter patológico.
Se sabe que un aumento crónico del cortisol o reactividad al estrés va a ocasionar una serie de eventos adversos que van a ser predictores en la consecución de este hambre emocional.
El hambre emocional es una condición que va a crear un contexto perfecto para el desarrollo de síndrome metabólico, en donde la exposición a largo plazo a estrés psicológico y físico pueden ser la demanda principal en la consecución de estas alteraciones metabólicas y que luego se diagnostican en obesidad, diabetes tipo II, entre otras afecciones cardio metabólicas (12).
Ejercicio físico y sus efectos positivos en un ambiente inflamatorio
Se sabe que un sujeto con síndrome metabólico se ve expuesto a un ambiente de inflamación de bajo grado. Al parecer el ejercicio físico produciría efectos anti-inflamatorios que podrían estar controlados por múltiples mecanismos.
Algunos de estos mecanismo estarían representados por una mayor producción de adrenalina, cortisol, hormona del crecimiento, prolactina, entre otras, las cuales tendrían efectos inmunomoduladores al influir en el tráfico y las funciones de los leucocitos, pérdida de grasa visceral, liberación y aumento de los niveles de miocinas antiinflamatorias por parte del músculo esquelético activo, entre otras funciones (13, 14).
Tanto la adrenalina como el cortisol aumentan rápidamente durante el ejercicio y una vez liberados, la adrenalina permite la activación de funciones secuenciales sobre la hormona liberadora de corticotropina por el hipotálamo, la hormona adrenocorticotrópica por la glándula pituitaria y, finalmente, el cortisol por las glándulas suprarrenales.
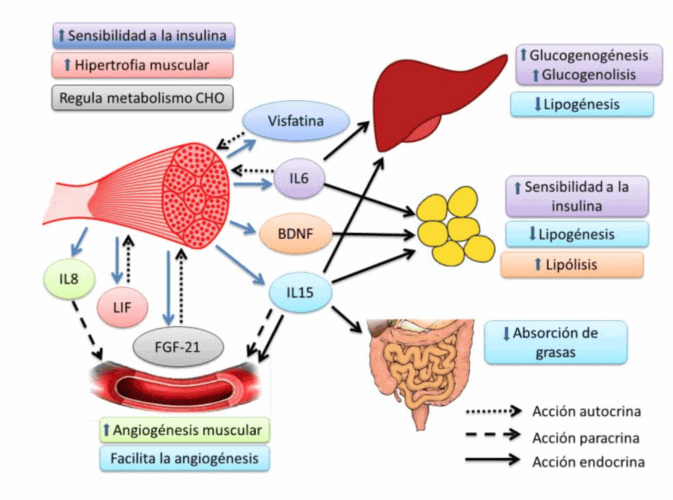
El aumento de los niveles plasmáticos de cortisol parece estar mediado en gran medida por la IL-6, miocina liberada por el músculo esquelético e inducido por el ejercicio físico en dependencia de la intensidad y duración del mismo (15).
Por otro lado, se evidencia que el ejercicio físico aumenta la producción y liberación de miocinas antiinflamatorias a partir de la contracción del músculo esquelético. Aunque no hay que confundir, el estrés crónico con los efectos positivos y beneficiosos que ejerce el ejercicio sobre el metabolismo de los adipocitos. Logrando a posterior, un ambiente altamente beneficioso y necesario para apaliar los efectos negativos, tanto físicos como psicológicos que producen el estrés crónico y el hambre emocional.
Conclusión sobre cortisol y hambre emocional
Al parecer el hambre emocional es producido en gran medida por un excesivo estrés psicológico que desencadena una cascada de desequilibrios hormonales y metabólicos. Estos desequilibrios ocasionan la liberación de cortisol que en gran medida favorecería y sensibilizaría a los mecanismos centrales encargados de producir placer producto del consumo de ciertos alimentos altamente palatables.
El hambre emocional entonces, puede crear un contexto propicio para el acceso a múltiples patologías cardio-metabólicas o enfermedades como la obesidad, diabetes tipo II y síndrome metabólico, es por eso, que debe ser tenido en cuenta y tratado como lo que es, una afección que genera consecuencias tanto desde lo físico como desde lo psicológico, de hecho se puede apreciar esto en las secuelas que dejó la pandemia actual COVID-19.
El ejercicio físico se presenta como una alternativa no farmacológica que produciría efectos positivos en este ambiente de ansiedad y depresión. Permitiendo que el organismo genere cortisol pero esta vez con una consecución de efectos que favorecen o conducen a procesos anti-inflamatorios y altamente positivos en un entorno en donde el tejido adiposo comienza a tomar el control.
Ver esta publicación en Instagram
Referencias bibliográficas
- Dressl, N. L. et al (2017). Cortisol como biomarcador de estres, hambre emocional y estado nutricional. Revista nutrición investiga. Universidad de Buenos Aires, Facultad de Medicina Buenos Aires, Argentina.
- Cortés Romero, C. E. et al. (2018). Stress and cortisol: implications on food intake. Revista Cubana de Investigaciones Biomédicas. ;37(3). (enlace)
- Paredes S, Ribeiro L. (2014). Cortisol: the villain in metabolic syndrome?. Revista da Associacao Medica Brasileira. 60(1), 84‐92. (enlace)
- Rosenkilde, M. et al. (1985). Appetite regulation in overweight, sedentary men after different amounts of endurance exercise: a randomized controlled trial. Journal of Applied Physiology. 115(11), 1599‐1609. (enlace)
- Goodpaster B. y Kelley D. (2008). Metabolic inflexibility and insulin resistance in skeletal muscle in: Hawley J. Zierath J. Physical Activity and Type 2 Diabetes. Human Kinetics, 59-66. (enlace)
- Randle, P. J., et al (1963). The glucose fatty-acid cycle. Its role in insulin sensitivity and the metabolic disturbances of diabetes mellitus. Lancet. 1963;1(7285), 785‐789. (enlace)
- Kelley, D.E., et al (1993). Interaction between glucose and free fatty acid metabolism in human skeletal muscle. The Journal of Clinical Investigation .92 (1): 91‐98. (enlace)
- Epel, E. et al. (2001). Stress may add bite to appetite in women: a laboratory study of stress-induced cortisol and eating behavior. Psychoneuroendocrinology. 26(1), 37‐49. (enlace)
- Torres, S. J. y Nowson, C. A. (2007). Relationship between stress, eating behavior, and obesity. Nutrition. 23(11-12), 887‐894. (enlace)
- Tataranni, P. A. et al (1996). Effects of glucocorticoids on energy metabolism and food intake in humans. The American Journal Physiology. 271 (21), 317‐ 325. (enlace)
- Dallman, M. F. et al (2003). Chronic stress and obesity: a new view of «comfort food». Proc Natl Acad Sci U S A. 100(20), 11696‐11701. (enlace)
- Cardi, V. et al (2015). The effects of negative and positive mood induction on eating behaviour: A meta-analysis of laboratory studies in the healthy population and eating and weight disorders. Neuroscience and Biobehavioral Reviews. 57: 299‐309. (enlace)
- Nieman, D. C. y Wentz, L. M. (2019). The compelling link between physical activity and the body’s defense system
Journal of Sport and Health Science. 8(3): 201–217. (enlace) - Pedersen, B. K. y Hoffman-Goetz, L. (2000). Exercise and the immune system: regulation, integration, and adaptation. Physiology Reviews. 80(3), 1055‐1081. (enlace)
- Wedell-Neergaard, A. S. et al (2019). Exercise-Induced Changes in Visceral Adipose Tissue Mass Are Regulated by IL-6 Signaling: A Randomized Controlled Trial. Cell Metabolism. 29(4):844‐855. (enlace)


Lic. Ortiz, Jonathan Nahuel
Interesante artículo, muy acertado, no cuestionaré el texto, así que solo haré un pequeño comentario de forma y tiene que ver con el uso de imágenes, la imagen número 3 es una imagen que yo hice y utilicé en la publicación de un artículo que publiqué hace algunos años. Role of the myokines production through the exercise. HH León, CE Melo, JF Ramírez
Journal of sport and health research 4 (2), 157-166.
En teoría cuando se hace esto es necesario solicitar un permiso para su uso y citar el artículo, pero no veo que ninguna de las dos cosas se hayan dado. Espero lo tengan en cuenta para futuras publicaciones.
Henry H. León A. MD. PhD.
Gracias por tu comentario compañero, estas cosas no deberían pasar. Ya se arregló la imagen y se colocó la referencia. Muchas gracias!!