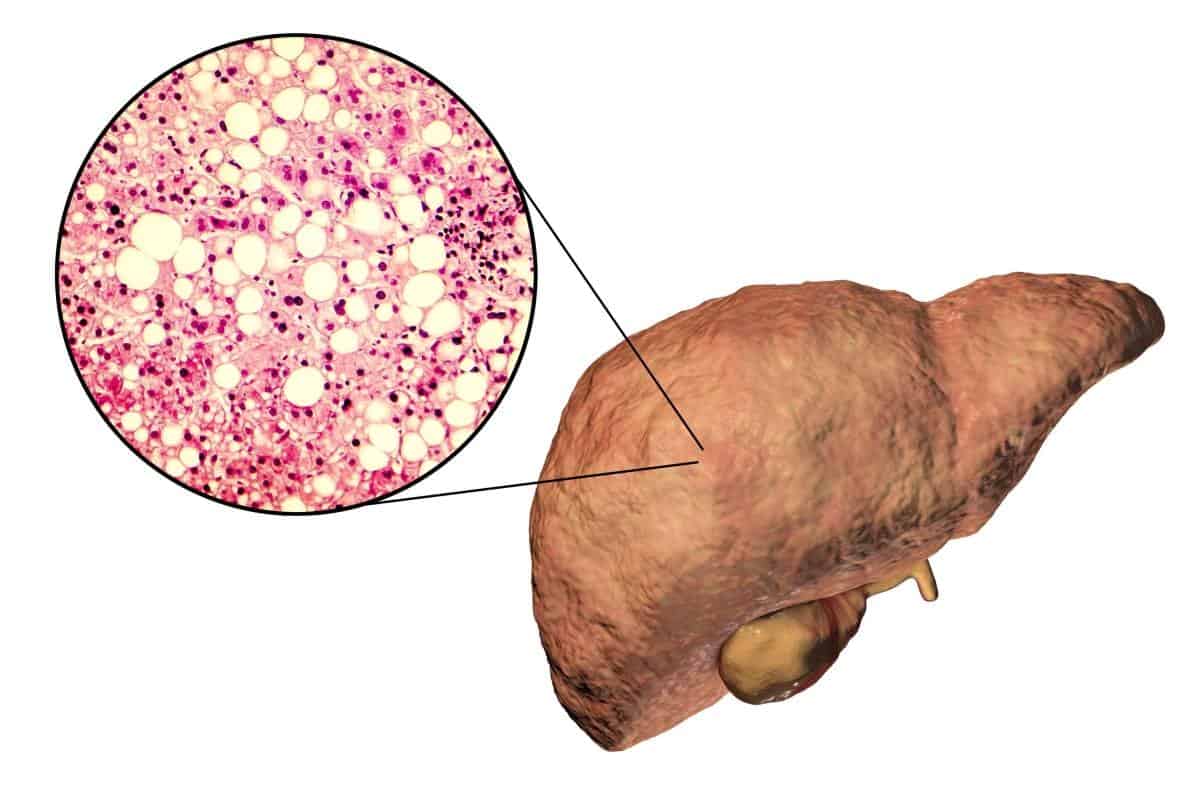
En este artículo vamos a analizar la n-acetilcisteína como un potente antioxidante que previene ciertas lesiones hepáticas.
Además, detallares en profundidad su eficacia y adversos para la salud, así como algunas de las preguntas más destacadas.
¿Qué es la N-acetilcisteína (NAC)?
La NAC es un potente antioxidante, que actúa directamente incrementado el GSH intracelular, especialmente en el tejido hepático (13).
La administración de N-acetilcisteína ha demostrado ser beneficiosa en diversas enfermedades como : enfermedades inflamatorias del intestino (14), enfermedades pulmonares, esclerosis sistémica, fibrosis quística, la infección por virus de la inmunodeficiencia humana (VIH), shock séptico, diabetes y lesiones hepáticas (15-16).
Eficacia de la N acetilcisteína
En el período del 2013 al 2014, se realizó una investigación doble ciego en un hospital con 60 pacientes intoxicados por acetaminofén.
Los pacientes se dividieron en 2 grupos de 30 personas, a un grupo se le administró N acetilcisteína, y al otro grupo se le administró N acetilcisteína con cimetidina; se midieron los niveles séricos de acetaminofén y las transaminasas en sangre al momento de ingreso al hospital y a las 4,12, 24 y 48 horas posteriores a su admisión.
En ambos grupos, los niveles de acetaminofén en sangre a las 48 horas fue de cero, por lo tanto, el tratamiento contra la toxicidad hepática fue exitoso, sin embargo, no hubo diferencias importantes entre la administración de N-acetilcisteína sola o en conjunto con cimetidina (3).
Otro estudio, encontró evidencia prometedora, sin embargo, los datos no mostraron diferencias significativas entre el grupo control y experimental.
En esta investigación se compararon 44 pacientes que recibieron N acetilcisteína con 44 pacientes que no recibieron N acetilcisteína después de una operación de resección hepática; se realizaron pruebas de función hepática en los días 1, 3 y 5 post-operación. El grado de insuficiencia hepática fue menor en el grupo que recibió N acetilcisteína, aunque esta diferencia no alcanzó significación estadística (18).Se realizó un reporte de un caso acerca de un paciente masculino de 45 años de edad, que ingresó con signos de necrosis hepatocelular e insuficiencia hepática, el paciente admitió haber utilizado cannabinoides sintéticos .
Las pruebas de intoxicación por paracetamol y alcohol resultaron negativas. Se administró de forma intravenosa N-acetilcisteína; el daño hepatocelular disminuyó y el paciente se recuperó por completo. Se han reportado otros intoxicaciones por el uso de esta droga pero no la toxicidad hepática (19).
Acetilcisteína y el hígado
El hígado cumple importantes funciones de desintoxicación en el cuerpo humano, existen diversos factores que pueden afectar el hígado y poner en riesgo la salud de las personas, algunos de estos factores son: enfermedades, drogas, fármacos, alcohol, químicos, etc.
Diversas investigaciones se han enfocado en encontrar formas de proteger o mejorar la salud del hígado, la Acetilcisteína es un producto que puede ayudar a mejorar el daño hepático inducido por intoxicación.
La toxicidad aguda por acetaminofén (paracetamol), es muy frecuente debido a su disponibilidad y a que posee una amplia gama de aplicaciones terapéuticas (1). Las sobredosis de acetaminofén son las causas más comunes de insuficiencia hepática en los Estados Unidos (1-7).Los efectos adversos de este fármaco son: náuseas, vómitos, diarrea, dolor abdominal y shock y se pueden producir de 4-14 horas después de la ingestión del medicamento, a partir de las 24-48 horas las aminotransferasas del hígado se incrementan, este incremento indica que existe daño hepático (7).
Cuando el acetaminofén se administra de forma oral el acetaminofén, éste es convertido principalmente en compuestos neutros e inofensivos por una reacción en el organismo (reacción tipo II) (4). Sin embargo,debido a una reacción tipo I (citocromo P450) una pequeña parte es convertida en un metabolito tóxico llamado N-acetyl-p-benzoquinoneimina (NAPQI), produciendo daño en los lóbulos hepáticos (8).
Existe una alta tasa de mortalidad por insuficiencia hepática, debido a la falta de viabilidad para el tratamiento. El uso de la acetilcisteína (NAC) se ha sugerido para el manejo de las intoxicaciones hepáticas (3).
Poder antioxidante
Los antioxidantes son compuestos naturales o sintéticos producidos in vivo, son constituyentes celulares y también se pueden obtener mediante la alimentación; su función principal es combatir el estrés oxidativo (9), de esta forma se puede retrasar o prevenir la oxidación de sustratos como proteínas, ácido desoxirribonucleico (ADN), lípidos, reducir el estrés oxidativo, combatir mutaciones del ADN, transformaciones malignas y otros parámetros de daño celular (10).
Debido a la importante función de los hepatocitos del hígado en el metabolismo de drogas, los xenobióticos (compuestos de origen sintético o natural que el organismo metaboliza y acumula y que pueden ser peligrosos para la salud) y compuestos endógenos, se requiere un importante sistema antioxidante (11).
Entre estos sistemas destaca el glutatión (GSH), el antioxidante más abundante en el organismo y que realiza funciones importantes protegiendo a las células de la toxicidad (12).
¿La acetilcisteína es segura? ¿Cuáles son sus efectos adversos?
Aunque su uso ha sido autorizado, tenemos que tener en cuenta una serie de contraindicaciones, destacando:
- Alergia al compuesto
- Ulcus gastroduodenal
- Asma bronquial o insuficiencia respiratoria grave (riesgo de aumento de la obstrucción de vías respiratorias).
- Niños menores de 2 años
Además, se han observados efectos secundarios como náuseas, vómitos, fiebre, cefaleas, tinnitus, somnolencia, mareo, reacción anafilactoide y broncoespasmo.
La Acetilcisteína, un gran protector hepático
Varios estudios han demostrado resultados positivos para el uso de la N acetilcisteína en lesiones hepáticas , principalmente en modelos animales (16).
Sin embargo, es necesario el aumento de investigaciones en humanos para que los profesionales de la salud puedan estar seguros acerca de la efectividad, seguridad, vía de administración, dosis optima y duración de la terapia de la N acetilcisteína.
Preguntas y respuestas frecuentes sobre la acetilcisteína
Aquí se muestran algunas de las preguntas más comunes sobre este potente antioxidante:
- ¿Qué es la acetilcisteína? Es un medicamento mucolítico que ayuda a disolver la mucosidad en las vías respiratorias y se usa en afecciones como la bronquitis y la EPOC.
- ¿Para qué se utiliza? Se usa para tratar afecciones respiratorias con exceso de mucosidad, intoxicaciones por paracetamol y como antioxidante en ciertas terapias.
- ¿Cómo se toma la acetilcisteína? Generalmente se toma en comprimidos efervescentes, cápsulas o solución oral, siguiendo las indicaciones médicas en cuanto a dosis y frecuencia.
- ¿Cuáles son los efectos secundarios de la acetilcisteína? Puede causar náuseas, vómitos, malestar estomacal, urticaria o, en raros casos, reacciones alérgicas graves.
- ¿Este suplemento es seguro durante el embarazo? Debe utilizarse con precaución y solo bajo supervisión médica, ya que no hay estudios concluyentes sobre su seguridad en el embarazo.
- ¿Puede la acetilcisteína ayudar en la desintoxicación del hígado? Sí, se usa en casos de intoxicación por paracetamol para proteger el hígado y ayudar en la eliminación de toxinas.
- ¿Es recomendable tomar acetilcisteína para la gripe o el resfriado? Puede ser útil para aliviar la mucosidad en casos de resfriado, pero no combate directamente el virus de la gripe.
- ¿La acetilcisteína tiene interacciones con otros medicamentos? Sí, puede interactuar con antibióticos, nitroglicerina y ciertos medicamentos para la presión arterial. Se recomienda consultar a un médico antes de tomarla junto con otros fármacos.»
Bibliografía
- Watson, W. A., Litovitz, T. L., Rodgers, G. C., Klein-Schwartz, W., Reid, N., Youniss, J., & Wruk, K. M. (2005). 2004 annual report of the American association of poison control centers toxic exposure surveillance system. The American journal of emergency medicine, 23(5), 589-666..
- Lee, W. M. (2004). Acetaminophen and the US Acute Liver Failure Study Group: lowering the risks of hepatic failure. Hepatology, 40(1), 6-9.
- Ebrahimi, M., Mousavi, S. R., Toussi, A. G., Reihani, H., & Bagherian, F. (2015). Comparing the Therapeutic Effectiveness of N-acetylcysteine with the Combination of N-acetyl Cysteine and Cimetidine in Acute Acetaminophen Toxicity: A Double-Blinded Clinical Trial. Electronic physician, 7(6), 1310.
- Ostapowicz, G., Fontana, R. J., Schiødt, F. V., Larson, A., Davern, T. J., Han, S. H., & Crippin, J. S. (2002). Results of a prospective study of acute liver failure at 17 tertiary care centers in the United States. Annals of internal medicine, 137(12), 947-954.
- Lee, W. M. (2003, August). Acute liver failure in the United States. Seminars in liver disease ,23 (3),217-226.
- Bessems, J. G., & Vermeulen, N. P. (2001). Paracetamol (acetaminophen)-induced toxicity: molecular and biochemical mechanisms, analogues and protective approaches. Critical Reviews in Toxicology, 31(1), 55-138.
- Goldfrank, L. R., Flomenbaum, N. E., Lewin, N. A., Weisman, R., Howland, M. A., & Hoffman, R.(1998). Goldfrank’s Toxicologic Emergencies. Stamford: Appleton & Lange.
- Laine, J. E., Auriola, S., Pasanen, M., & Juvonen, R. O. (2009). Acetaminophen bioactivation by human cytochrome P450 enzymes and animal microsomes. Xenobiotica, 39(1), 11-21.
- Musacco-Sebio, R., Saporito-Magriñá, C., Semprine, J., Torti, H., Ferrarotti, N., Castro-Parodi, M., & Repetto, M. G. (2014). Rat liver antioxidant response to iron and copper overloads. Journal of inorganic biochemistry, 137, 94-100.
- Pisoschi, A. M., & Pop, A. (2015). The role of antioxidants in the chemistry of oxidative stress: A review. European journal of medicinal chemistry, 97, 55-74.
- Chen, Y., Johansson, E., Yang, Y., Miller, M. L., Shen, D., Orlicky, D. J., & Dalton, T. P. (2010). Oral N-acetylcysteine rescues lethality of hepatocyte-specific Gclc-knockout mice, providing a model for hepatic cirrhosis. Journal of hepatology, 53(6), 1085-1094.
- Chen, Y., Dong, H., Thompson, D. C., Shertzer, H. G., Nebert, D. W., & Vasiliou, V. (2013). Glutathione defense mechanism in liver injury: insights from animal models. Food and chemical toxicology, 60, 38-44.
- Ribeiro, G., Roehrs, M., Bairros, A., Moro, A., Charão, M., Araújo, F., & Leal, M. (2011). N-acetylcysteine on oxidative damage in diabetic rats. Drug and chemical toxicology, 34(4), 467.
- Moura, F. A., de Andrade, K. Q., dos Santos, J. C., Araújo, O. R., & Goulart, M. O. (2015). Antioxidant therapy for treatment of inflammatory bowel disease: Does it work?. Redox biology, 6, 617-639.
- Li, J., Zhang, S., Wu, Y., Guo, W., Zhang, Y., & Zhai, W. (2010). Protective effects of N-acetylcysteine on the liver of brain-dead Ba-Ma mini pig. In Transplantation proceedings,42(1),195).
- de Andrade, K. Q., Moura, F. A., dos Santos, J. M., de Araújo, O. R. P., de Farias Santos, J. C., & Goulart, M. O. F. (2015). Oxidative Stress and Inflammation in Hepatic Diseases: Therapeutic Possibilities of N-Acetylcysteine. International journal of molecular sciences, 16(12), 30269-30308.
- Singh, S., Hynan, L. S., & Lee, W. M. (2013). Improvements in Hepatic Serological Biomarkers Are Associated with Clinical Benefit of Intravenous N-Acetylcysteine in Early Stage Non-Acetaminophen Acute Liver Failure. Digestive Diseases and Sciences, 58(5), 1397.
- Robinson, S. M., Saif, R., Sen, G., French, J. J., Jaques, B. C., Charnley, R. M.,& White, S. A. (2013). N‐acetylcysteine administration does not improve patient outcome after liver resection. The official Journal of the International Hepato Pancreato Biliary Association, 15(6), 457-462.
- Sheikh, I. A., Lukšič, M., Ferstenberg, R., & Culpepper-Morgan, J. A. (2014). SPICE/K2 Synthetic Marijuana-Induced Toxic Hepatitis Treated with N-Acetylcysteine. The American journal of case reports, 15, 584.