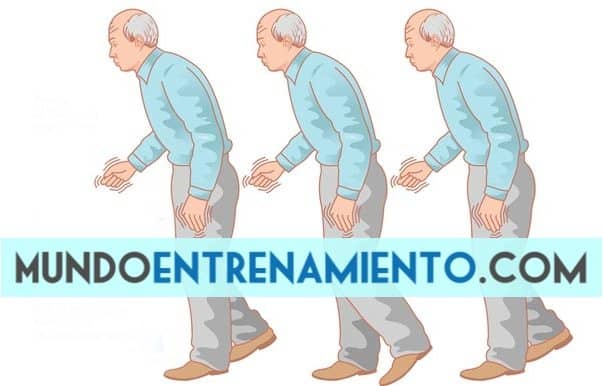
La Enfermedad de Parkinson (EP) es un trastorno neurodegenerativo que afecta al sistema nervioso, produciéndose unos mecanismos de daño y posterior degeneración de las neuronas ubicadas en la sustancia negra. Estas neuronas se encargan de producir la dopamina (neurotransmisor) fundamental para que el movimiento del cuerpo se realice correctamente.
La alteración del patrón de marcha normal, causada por los síntomas, como la acinesia y la pérdida de los reflejos posturales, es un problema en los pacientes con EP. (1).
La marcha característica de la EP sigue un patrón de marcha hipocinética-rígida. En ella existe una pérdida de las sinergias entre la postura-locomoción que da lugar a una postura en la flexión del tronco y de las articulaciones, disminución del braceo; disminución de la altura y longitud del paso (lo que se traduce en la aparición de la festinación), presencia de giros en bloque, acortamiento del paso y reducción en la velocidad (que se convierte en una de las principales características del patrón de la marcha), fundamentalmente debida al acortamiento de la longitud de la zancada (4).
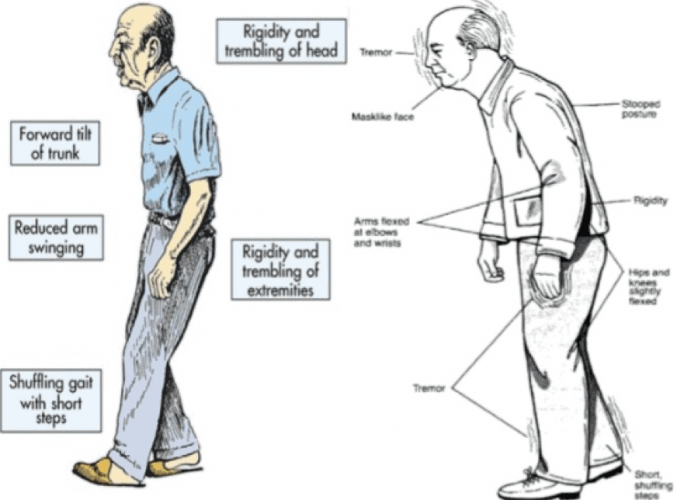
La cadencia puede permanecer inalterada o estar aumentada en algunos casos como resultado de mecanismos compensatorios (2,3,4). Debido al papel que desempeñan los ganglios basales en el inicio y la regulación de los programas motores, el doble apoyo y el ciclo de la marcha se encuentran afectados (5).
Además, destaca la presencia de una pérdida de la actividad muscular programada. En general, la marcha en pacientes con parkinson puede mejorar con ayudas externas y empeorar con la realización de una tarea simultánea (dual tasking) (6).
Los trastornos de la marcha en pacientes con parkinson en fases finales se presentan hasta en un 80% de los pacientes (7). En un estudio de 2014 que tenía por objetivo priorizar las 10 primeras incertidumbres que influían en la práctica clínica diaria en la EP, se identificaron los trastornos de la marcha, el equilibrio y las caídas como primeras prioridades que necesitan ser investigadas con el objetivo de intentar mejorar las posibilidades terapéuticas de la EP (8).
A pesar del impacto de la alteración de la marcha en la calidad de vida de muchos pacientes con EP, que les hace ser más dependientes y se relaciona con mayor riesgo de caídas (9), destaca la escasa repercusión que tiene la marcha en la mayoría de las escalas de valoración de la EP. Además, su evaluación se basa fundamentalmente en un análisis visual poco preciso y objetivo, como ocurre en la Unified Parkinson’s Disease Rating Scale (10).
Aunque, existen una serie de biomarcadores reconocidos para la identificación y evaluación de la EP en los que respecta a su clínica neurológica y complicaciones, en la actualidad han surgido métodos objetivos para medir el movimiento y analizar con datos cuantitativos, la acción del aparato locomotor, los cuales pueden proporcionar un complemento adicional a la hora de la toma de decisiones clínicas (7).
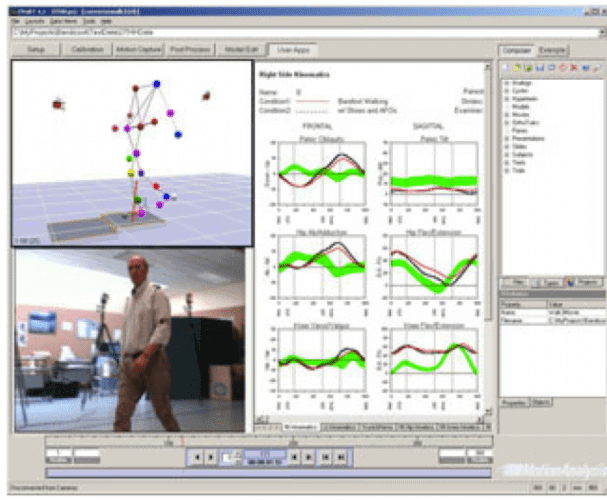
Como es ya sabido la marcha en pacientes con parkinson /strong> se ve perturbada, por lo cual la gran mayoría de las medidas para evaluar este parámetro temporal serian poco sensibles. Por lo tanto los parámetros que no se basen sólo en la cadencia de la marcha podrían ser utilizados para analizar la degeneración motora de la enfermedad y sus consecuencias sobre la marcha del paciente con parkinson (13). En un intento por analizar parámetros derivados de la cinemática, en busca de una mejora en el entendimiento de los procesos motores durante la marcha, se ha investigado una serie de medidas cuantitativas tanto espaciales como temporales que son evaluadas en laboratorios de marcha con el empleo de material tecnológico y programas de datos (FIG.2):
- Frecuencia de ciclos con secuencia normal (HFPS): heel strike (fase de frenada), foot contact (fase de apoyo), push off (fase de empuje) y swing (fase de oscilación).
- Número de ciclos totales.
- Cadencia.
- Porcentaje de apoyo monopodal y bipodal.
- Porcentaje de duración de las fases de la marcha.
- Rango articular de la rodilla y del tobillo (tomando como dato los grados de diferencia entre el grado máximo y mínimo que se registra).
- Activación muscular.
Dentro de un mismo paciente, podemos encontrar una gran variabilidad de secuencias de apoyo (que define las fases del paso), a diferencia de lo que sucede en sujetos normales, en los que la gran mayoría de los pasos sigue una misma secuencia. Como hecho novedoso últimos estudios destacan que la proporción de ciclos con la secuencia de apoyo correcta (HFPS) se encuentra marcadamente reducida en los pacientes con EP avanzada –siendo ésta del 67%– incluso bajo medicación.
Se encuentra además un aumento del número total de ciclos y alteración de la cadencia en muchos pacientes, y conservación de la cadencia media dentro de los límites de la normalidad, aumento de la duración de la fase de apoyo, disminución del apoyo monopodal y alteración del rango articular de la rodilla y el tobillo (11).
Asimismo, se puede observar una alteración en las puntuaciones obtenidas en las escalas clínicas, que mostraban un aumento del factor de riesgo de caídas y dependencia leve. Se ha demostrado en otros estudios que la levodopa mejora los parámetros de longitud de zancada, la velocidad, el rango articular de la cadera, la rodilla y el tobillo, y el tiempo del doble apoyo (12).
Por ello, se podría inferir que, si se estudiaran pacientes no medicados, al comparar con los valores de la normalidad de los estudios cuantitativos de la marcha con gran probabilidad nos encontraríamos con una mayor afectación en los pacientes con EP avanzada.
Este mismo argumento se podría utilizar respecto a comparación con la normalidad de la puntuación de las escalas clínicas. Dejando sobre la mesa muchísimas hipótesis sobre el tema, pero haciendo un sondeo general de los artículos y la literatura actual, se puede concluir que en un futuro muy cercano la cuantificación mediante análisis objetivo de las variables cinéticas y cinemáticas en los pacientes con EP se empleara como herramienta rutinaria para establecer la influencia de las distintas alternativas terapéuticas.
Bibliografía
- Hausdorff, J. M. (2009). Gait dynamics in Parkinson’s disease: common and distinct behavior among stride length, gait variability, and fractal-like scaling. Chaos 19, 026113. doi: 10.1063/1.3147408
- Stern GM, Franklyn SE, Imms FJ, Prestidge SP. (1983). Quantitative assessments of gait and mobility in Parkinson’s disease. J Neural Transm Suppl 19: 201-14.
- Murray MP, Sepic SB, Gardner GM, Downs WJ. (1978). Walking patterns of men with parkinsonism. Am J Phys Med; 57: 278-94
- Moreau C, Cantiniaux S, Delval A, Defebvre L, Azulay JP. (2010). Gait disorders in Parkinson’s disease: and pathophysiological approaches. Rev Neurol (Paris); 166: 158-67.
- Schepens B, Stapley P, Drew T. (2008). Neurons in the pontomedullary reticular formation signal posture and movement both as an integrated behavior and independently. J Neurophysiol; 100: 2235-53.
- Yogev-Seligmann G, Giladi N, Gruendlinger L, Hausdorff JM. (2013). The contribution of postural control and bilateral coordination to the impact of dual tasking on gait. Exp Brain Res; 226: 81-93
- Giladi N, Treves TA, Simon ES, Shabtai H, Orlov Y, Kandinov B, et al. (2001). Freezing of gait in patients with advanced Parkinson’s disease. J Neural Transm; 108: 53-61.
- Deane KHO, Flaherty H, Daley DJ, Pascoe R, Penhale B, Clarke CE, et al. (2014). Priority setting partnership to identify the top 10 research priorities for the management of Parkinson’s disease. BMJ Open; 4: e006434.
- Giladi N. (2008). Medical treatment of freezing of gait. Mov Disord; 23 (Suppl 2): S482-8.
- Mera TO, Filipkowski DE, Riley DE, Whitney CM, Walter BL, Gunzler SA, et al. (2013). Quantitative analysis of gait and balance response to deep brain stimulation in Parkinson’s disease. Gait Posture; 38: 109-14.
- Villadóniga M, San Millán A, Cabañes-Martínez L, Avilés-Olmos I, Del Álamo-De Pedro M, Regidor I. (2016). Análisis cuantitativo de la marcha en pacientes con Parkinson avanzada. Rev Neurol; 63: 97-102.
- Luquin MR, García-Ruiz PJ, Martí MJ, Rojo A, Vela L, Grandas FJ, et al. (2012). Levodopa en el tratamiento de la enfermedad de Parkinson: mitos y realidades. Rev Neurol 55: 669-88.
- König N, Singh NB, Baumann CR and Taylor WR (2016) Can Gait Signatures Provide Quantitative Measures for Aiding Clinical Decision-Making? A Systematic Meta-Analysis of Gait Variability Behavior in Patients with Parkinson’s Disease. Front. Hum. Neurosci. 10:319. doi: 10.3389/fnhum.2016.00319.
GERARDO ALONSO PEDRAJA ANDRADE. Estudiante del Máster en Entrenamiento Deportivo, Actividad Física y Salud. Facultad de Psicología, Ciencias de la Educación y del Deporte Blanquerna-Universidad Ramon Llull